Содержание
Как создать клон
Как клонировать животное? Как клонировать человека? Как клонировать растение? Как клонировали овечку Долли? И что такое клон?
Как создать клон?
Как известно, в процессе размножения большинства высших организмов, дочерняя особь получает половину генов от отца, а половину — от матери, то есть отличается по генотипу (набору генов) как от отца, так и от матери.
Клонами в биологии называют организмы, имеющие одинаковый генотип.
Следует помнить, что получить при клонировании абсолютно точную копию практически невозможно – в процессе индивидуального развития часть генов может «работать», а часть «молчать», на активацию тех или иных генов могут влиять внешние факторы.
Как клонировать животное?
Первые успешные опыты по клонированию животных были проведены в середине 1970-х годов английским эмбриологом Дж. Гордоном, когда путем пересадки ядра клетки головастика в икринку лягушки был получен новый головастик.
Значительный вклад в решение проблемы клонирования млекопитающих внесен шотландской группой исследователей из Рослинского института и компании «PPL Therapeuticus» под руководством Яна Вилмута. В 1996 году появились их публикации по успешному рождению овец Меган и Морган в результате переноса ядер клеток овечьих эмбрионов в неоплодотворенные яйцеклетки овцы. В 1997 году группой Вилмута было использовано ядро взрослой (а не эмбриональной) клетки и получена овца по имени Долли.
В случае Долли применялась та же технология переноса ядра, что и при клонировании животных из эмбриональных клеток.
В процессе переноса используются две клетки. Клетка-реципиент — неоплодотворенная яйцеклетка, клетка-донор берется у клонируемого животного. В случае овечек Меган и Морган клетки-доноры брали из овечьих эмбрионов, в случае Долли использовались дифференцированные (взрослые) клетки из нижней части вымени овцы, находившейся на четвертом месяце беременности. Беременное животное было выбрано потому, что у беременной овцы вымя активно растет, то есть его клетки активно делятся и отличаются повышенной жизнеспособностью.
С использованием микроскопа и двух тончайших каппилляров из клетки — реципиента удаляется ДНК, затем донорская клетка, содержащая ядро с хромосомной ДНК, соединяется с лишенной генетического материала яйцеклеткой-реципиентом.
После этого некоторые из слитых клеток начинают делиться, а после помещения их в матку суррогатной матери развиваться в эмбрион.
По сообщениям специалистов Института Рослина, нормально развивается лишь один из тридцати эмбрионов, подсаженных суррогатным матерям.
В дальнейшем обнаружилось, что «нормально развивавшаяся» клонированная овца Долли стареет в несколько раз быстрее своих «нормально рожденных» родственников. Согласно одному из наиболее вероятных объяснений, старение происходит в силу запрограммированного ограничения количества делений и продолжительности жизни каждой клетки высших организмов. По одной из версий это определяется длиной концевых участков плеч хромосом — теломерных повторов. При каждом делении клетки их длина уменьшается, что, соответственно и определяет оставшееся разрешенное клетке время жизни. Поскольку в качестве донорской при создании Долли использовалась клетка уже взрослого животного, которая претерпела до этого, по крайней мере, несколько делений, теломеры ее хромосом к тому времени были несколько укорочены, что и могло определить общий биологический возраст клонированного организма.
Как клонировать человека?
С тех пор как появилась на свет клонированная овца, во всем мире не умолкают споры о необходимости запрета или разрешении клонирования человека.
При этом следует помнить, что организмами с идентичным генотипом, то есть природными клонами, являются однояйцовые близнецы. Так и искусственно полученный «клон» человека будет являться лишь младшим во времени близнецом донора ДНК. Так же, как и у близнецов, у клона и донора ДНК будут разные отпечатки пальцев. Клон не унаследует ничего из воспоминаний оригинального индивида.

Как клонировать растение?
Клонирование растений, в отличие от клонирования животных, является обычным процессом, с которым сталкивается любой цветовод или садовод. Когда растение размножают отростками, черенками, усиками — это и есть пример клонирования. Именно так и получается новое растение с генотипом, идентичным растению-донору побега. Это возможно благодаря тому, что у растений по мере роста клетки не теряют возможность реализовывать всю генетическую информацию, заложенную в ядре.
История клонирования животных
МИНОБРНАУКИ РОССИИ
Федеральное государственное автономное образовательное
учреждение высшего образования
«ЮЖНЫЙ ФЕДЕРАЛЬНЫЙ УНИВЕРСИТЕТ»
РЕФЕРАТ
на тему:
ИСТОРИЯ КЛОНИРОВАНИЯ ЖИВОТНЫХ
Выполнил:
студентка 4 курса
химического факультета
Терещенко Татьяна Александровна.
Проверил:
преподаватель кафедры биохимии и микробиологии
Аллилуев Илья Александрович
Ростов-на-Дону
2017
Введение……………………………………………………………….3
-
Из истории исследований по клонированию животных…….4-6
-
Клонирование животных………………………………………7-9
-
Клонирование с целью воссоздания вымерших видов……..10-11
3.1Клонирование бантенгов
3.2Императорский дятел
3.3 Дронт
3.4Клонирование гигантских птиц
4. Применения клонов животных.………………………………12
Заключение…………………………………………………….…….13
Список литературы…………………………………………………14-15
Введение
Последние десятилетия XX века ознаменовались бурным развитием одной из главных ветвей биологической науки — молекулярной генетики. Уже в начале 70-х годов ученые в лабораторных условиях начали получать и клонировать рекомбинантные молекулы ДНК, культивировать в пробирках клетки и ткани растений и животных. Возникло новое направление генетики — генетическая инженерия. На основе ее методологии начали разрабатываться различного рода биотехнологии, создаваться генетически измененные организмы (ГМО). Появилась возможность генной терапии некоторых заболеваний человека, а последнее десятилетие XX века ознаменовалось еще одним важным событием — достигнут огромный прогресс в клонировании животных из соматических клеток.
Разработанные методы клонирования животных пока еще далеко не совершенны. В процессе экспериментов наблюдается высокая смертность плодов и новорожденных. Еще не ясны многие теоретические вопросы клонирования животных из отдельной соматической клетки. Тем не менее, многие ученые с энтузиазмом восприняли идею клонирования человека. Опрос общественного мнения в США показал, что 7% американцев готовы подвергнуться клонированию. Вместе с тем, большинство ученых и многие политики высказываются против создания клонов человека. И их возражения и опасения вполне оправданы.
-
Из истории исследований по клонированию животных
Возможность клонирования животных доказал Дж. Гердон, английский биолог, который первым сумел получить клонированные эмбрионы шпорцевых лягушек. Он выжигал ультрафиолетом ядра икринок и затем подсаживал в них ядра, выделенные из клеток эпителия головастиков этого вида. Большая часть полученных таким образом икринок погибала, и лишь совсем маленькая их доля (2,5%) развивалась в головастиков. Взрослых лягушек получить таким образом не удавалось. Тем не менее это был успех, и результаты опытов Гердона попали во многие учебники и руководства по биологии.
В 1976 г. Гердон и его соавтор Р. Ласки публикуют работу, в которой описывают опыты с ядрами, выделенными из клеток почек, кожи и легкого уже взрослых шпорцевых лягушек. Исследователи сначала подращивают эти клетки вне организма (in vitro), а затем вводят их ядра в безъядерные икринки. Четверть таких икринок начинает делиться, но вскоре замирает на одой из стадий развития. Тогда ученые выделяют ядра полученных эмбрионов и снова подсаживают их в лишенные собственных ядер икринки. В результате целой серии подобных пересадок на свет наконец-то появляется несколько головастиков.
Хотя эксперименты Гердона и его последователей показали принципиальную возможность получения серийных клонов амфибий, появляющиеся на свет головастики упорно не желали превращаться во взрослых лягушек. Вопрос, таким образом, по-прежнему заключался в том, можно ли вырастить из одной специализированной клетки его тела взрослое позвоночное животное. Опыты на амфибиях давали отрицательный результат, но ученые не прекращали исследований в этой области.
Более широкие исследования, охватывающие не только амфибий, но и рыб, а также дрозофил, в 1962 г. были начаты английским биологом Дж. Гордоном. Он первым в опытах с южноафриканскими жабами Xenopus laevis) в качестве донора ядер использовал не зародышевые клетки, а уже вполне специализировавшиеся клетки эпителия кишечника плавающего головастика.
Затем Гердон вместе с Ласки (1970) стали культивировать in vitro (вне организма в питательной среде) клетки почки, легкого и кожи взрослых животных и использовать уже эти клетки в качестве доноров ядер. Примерно 25% первично реконструированных яйцеклеток развивались до стадии бластулы. При серийных пересадках они развивались до стадии плавающего головастика. Таким образом было показано, что клетки трех разных тканей взрослого позвоночного (X. laevis) содержат ядра, которые могут обеспечить развитие по крайней мере до стадии головастика.
В свою очередь Ди Берардино и Хофнер (1983) использовали для трансплантации ядра неделящихся и полностью дифференцированных клеток крови — эритроцитов лягушки Rana pipiens. После серийной пересадки таких ядер 10% реконструированных яйцеклеток достигали стадии плавающего головастика. Эти эксперименты показали, что некоторые ядра соматических клеток способны сохранять тотипотентность.
Причины, по которым ядра клеток взрослых животных и даже поздних эмбрионов остаются тотипотентными, пока точно не установлены. Решающую роль играет взаимодействие ядра и цитоплазмы. Содержащиеся в цитоплазме животных вещества принимают участие в регулировании экспрессии клеточного генов ядра.
Работы М. ди Бернардино и Н. Хоффера показали, что цитоплазма ооцитов амфибий содержит факторы, восстанавливающие тотипотентность ядер дифференцированных соматических клеток. Эти факторы реактивируют репрессированные участки генома.
В 1985 г. была описана технология клонирования костных рыб, разработанная советскими учеными Л.А. Слепцовой, Н.В. Дабагян и К.Г.Газарян. Зародыши на стадии бластулы отделяли от желтка. Ядра клеток зародышей впрыскивали в цитоплазму неоплодотворенных икринок, которые начинали дробиться и развивались в личинки. Эти эксперименты показали, что потеря ядром тотипотентности в процессе онтогенеза связана не с утерей генов, а их репрессией. При культивировании соматических клеток in vitro частота тотипотентности ядер увеличивается. Генетический механизм стабильной репрессии генома дифференцированных клеток не выяснен, способы восстановления тотипотентности не разработаны, поэтому в основном ведется клонирование путем трансплантации ядер эмбриональных клеток.
Пересадки ядер у млекопитающих начались позднее, в 80-х годах. Это было связано с техническими трудностями, так как зигота млекопитающих имеет небольшие размеры. Например, диаметр зиготы мыши приблизительно 60 мкм, а диаметр оплодотворенной яйцеклетки лягушки около 1200 мкм, т.е. в 20 раз больше.
Несмотря на перечисленные трудности, первые сообщения о получении клонов мышей, идентичных донору, появились уже в 1981 году. В качестве донора были использованы эмбриональные клетки одной из линий мышей, взятые на стадии бластоцисты. Достоверность полученных данных вначале была поставлены под сомнение, так как воспроизвести результаты проведенных экспериментов в других лабораториях не удавалось, однако пару лет спустя Дж. Мак Грат и Д. Солтер также достигли успеха. В этих экспериментах клоны мышей удавалось получить лишь в том случае, если трансплантировали ядра эмбрионов на стадии не позднее 2 бластомеров. Было показано, что ядра 8-клеточных зародышей и клеток внутренней клеточной массы бластоцисты не обеспечивают развитие in vitro реконструированных яйцеклеток даже до стадии морулы, которая предшествует стадии бластоцисты. Небольшая часть (5%) ядер 4-клеточных зародышей дает возможность развиваться только до стадии морулы. Эти и многие другие данные показывают, что в эмбриогенезе у мышей клеточные ядра рано теряют тотипотентность, что связано очевидно, с очень ранней активацией генома зародыша — уже на стадии 2-х клеток. У других млекопитающих, в частности, у кроликов, овец и крупного рогатого скота, активация первой группы генов в эмбриогенезе происходит позднее, на 8-16-клеточной стадии. Возможно поэтому первые значительные успехи в клонировании эмбрионов были достигнуты на других видах млекопитающих, а не на мышах. Тем не менее, работы с мышами, несмотря на их непростую судьбу, значительно расширили наши представления о методологии клонирования млекопитающих.
В начале пути
1883 — Открытие яйцеклетки немецким цитологом Оскаром Гертвигом.
1943 — Журнал Science сообщил об успешном оплодотворении яйцеклетки «в пробирке».
1977 — Профессор зоологии Оксфордского университета Дж. Гордон клонирует более полусотни лягушек.
1978 — Рождение в Англии Луизы Браун, первого ребёнка «из пробирки».
1985 — 4 января в одной из клиник северного Лондона родилась девочка у миссис Коттон — первой в мире суррогатной матери (зачата не из яйцеклетки миссис Коттон).
1987 — Специалисты Университета имени Дж. Вашингтона, использовавшие специальный фермент, сумели разделить клетки человеческого зародыша и клонировать их до стадии тридцати двух клеток (бластов, бластомеров).
2. Клонирование животных
В своем эксперименте Кэмпбелл и его коллеги извлекли из эмбриона овцы на ранней стадии развития (на стадии эмбрионального диска) клетку и вырастили культуру клеток, то есть добились того, что клетка размножилась в искусственной питательной среде. Полученные генетически идентичные клетки (клеточная линия) сохранили тотипонентность. Затем ученые взяли яйцеклетку овцы-реципиента, тщательно удалили из нее весь хромосомный материал и добились ее слияния с тотипотентной клеткой из культуры. Полученные синтетические эмбрионы выращивали до стадии морулы-бластулы, а затем имплантировали в матку овцы. В результате удалось вырастить нескольких нормальных ягнят, которые были генетически идентичны.
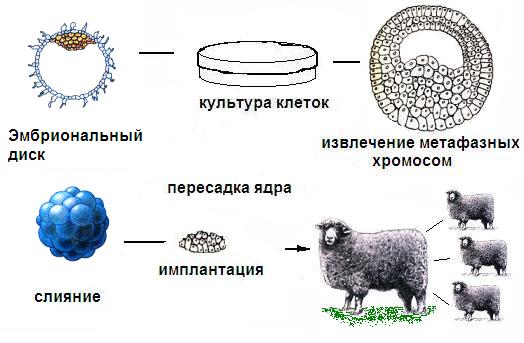
Рис.1. Методика, с помощью которой Кэмпбелл и его коллеги клонировали овец.
Из клеток эмбрионального диска получили устойчивые культуры клеток. Из ооцитов-реципиентов удаляли часть цитоплазмы вместе с метафазной пластинкой и индуцировали слияние таких безъядерных ооцитов с клеткой из тотипотентной клеточной линии. Полученные таким образом эмбрионы временно помещались в овцу-реципиента. через неделю проверяли уровень их развития. Наконец, морулы и бластоцисты имплантировались другим овцам, где и проходил весь онтогенез.
В принципе, после того, как получена устойчивая линия тотипонентных клеток, ничто не мешает вносить в них генетические изменения. Например, перестраивая или удаляя отдельные гены, можно создавать трансгенные линии овец и других сельскохозяйственных животных. Однако прежде чем эта технология найдет практическое применение, предстоит решить еще множество проблем.
Пока число клонированных животных очень мало по сравнению с числом исходных эмбрионов, из клеток которых удавалось получить культуру. Многие клетки погибали, не успев достичь стадии бластоцисты. Не ясно, вызван ли высокий процент неудач разнообразными вредными факторами, воздействующими на клетку при манипуляциях с нею, или гетерогенностью самой клеточной линии. Последнее менее вероятно, поскольку процент успешных случаев не меняется при пересевах культуры. Для прояснения этого вопроса необходимо исследовать другие тотипотентные клеточные линии.
Результативность пересадки ядра в яйцеклетку и ее последующее благополучное развитие зависит от адекватного перепрограммирования ядра донора. Макромолекулы (белки и транспортная РНК) ооцита отвечают за его развитие только в течение сравнительно короткого времени (между двумя клеточными делениями), и чем этот период короче, тем меньше остается времени для перепрограммирования. Клетки более зрелых эмбрионов требуют большего времени для перепрограммирования, поэтому вероятность успеха при их использовании снижается. Определенную роль играет также совместимость ядра донора и цитоплазмы реципиента, все еще слабо изученная.
Успех пересадки клеточных ядер связан по крайней мере с двумя факторами. Во-первых, овулировавшие ооциты являются лучшими реципиентами, чем зиготы, либо потому, что у неоплодотворенных яйцеклеток остается больше времени для перепрограммирования, либо потому, что их цитоплазма является более подходящей. Возможно, в цитоплазме ооцита есть элементы, необходимые для перестройки хромосом и активации генома и исчезающие после оплодотворения либо потому, что они каким-то образом связаны с реплицирующейся ДНК, либо в результате запрограммированного распада. Во-вторых, клетки с ядрами донора, взятыми на стадиях G1 или G0 клеточного цикла, развиваются гораздо лучше, чем клетки с ядрами со стадий S или G2 . Интуитивно это кажется понятным, ведь перепрограммировать открытый реплицирующийся геном проще.
Клонирование животных возможно с помощью экспериментальных манипуляций с яйцеклетками (ооцитами) и ядрами соматических клеток животных in vitro и in vivo подобно тому, как в природе появляются однояйцевые близнецы. Клонирование животных достигается в результате переноса ядра из дифференцированной клетки в неоплодотворённую яйцеклетку, у которой удалено собственное ядро (энуклеированная яйцеклетка) с последующей пересадкой реконструированной яйцеклетки в яйцевод приёмной матери. Однако долгое время все попытки применить описанный выше метод для клонирования млекопитающих были безуспешными. Значительный вклад в решение этой проблемы был сделан шотландской группой исследователей из Рослинского института и компании «PPL Therapeuticus» (Шотландия) под руководством Яна Вильмута. В 1996 году появились их публикации по успешному рождению ягнят в результате трансплантации ядер, полученных из фибробластов плода овцы, в энуклеированные ооциты.
В окончательном виде проблема клонирования животных была решена группой Вильмута в 1997, когда родилась овца по кличке Долли — первое млекопитающее, полученное из ядра взрослой соматической клетки: собственное ядро ооцита было заменено на ядро клетки из культуры эпителиальных клеток молочной железы взрослой лактирующей овцы. 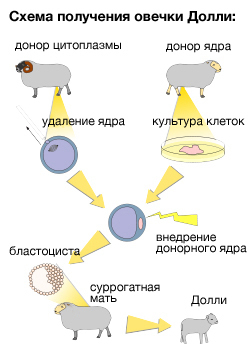
Рис 2. Схема получения овечки Долли
В дальнейшем были проведены успешные эксперименты по клонированию различных млекопитающих с использованием ядер, взятых из взрослых соматических клеток животных (мышь, коза, свинья, корова), а также взятых у мёртвых, замороженных на несколько лет, животных. Появление технологии клонирования животных вызвало не только большой научный интерес, но и привлекло внимание крупного бизнеса во многих странах. Подобные работы ведутся и в России, но целенаправленной программы исследований не существует. В целом технология клонирования животных ещё находится в стадия развития. У большого числа полученных таким образом организмов наблюдаются различные патологии, приводящие к внутриутробной гибели или гибели сразу после рождения.
В апреле 2008 года Южнокорейские таможенники приступили к дрессировке семи щенков, клонированных из соматических клеткок лучшего корейского розыскного пса породы канадский лабрадор-ретривер. По мнению южнокорейских ученых, 90 % клонированных щенков будут удовлетворять требованиям для работы на таможне, тогда как лишь менее 30 % обычных щенков проходят тесты на профпригодность.
3.Клонирование с целью воссоздания вымерших видов
Клонирование может быть использовано для воссоздания естественных популяций животных, вымерших по вине человека. Несмотря на наличие определённых проблем и трудностей, первые результаты в данном направлении уже имеются.
3.1Клонирование бантенгов
В 2004 году на свет появилась пара бантенгов (диких быков, обитавших в Юго-Восточной Азии), клонированных из клеток животных, умерших более 20 лет назад. Два бантенга были клонированы из уникального «замороженного зоопарка» Сан-Диего, созданного еще до того, как люди поняли, что клонирование вообще возможно. Произведшая клонирование американская компания Advanced Cell Technology сообщила, что в нем использовались клетки животных, которые умерли в 1980 году, не оставив потомства.
Бантенгов клонировали, перенеся их генетический материал в пустые яйцеклетки обычных домашних коров; из 16 зародышей до рождения дожили только два.
3.2Императорский дятел
В последний раз императорского дятла видели в Мексике в 1958 году. С тех пор орнитологи пытаются найти следы этой популяции, но безуспешно. Около десяти лет назад появились даже слухи, что птица еще живет на планете, но и они не подтвердились.
Зато в музеях остались чучела птицы. Научный сотрудник Дарвиновского музея Игорь Фадеев считает, что если операцию по выделению ДНК провести со всеми чучелами, которые находятся в разных странах мира, то дятла можно будет воскресить. В разных музеях мира на сегодняшний день осталось лишь десять чучел императорского дятла.
Если проект увенчается успехом, то в недалеком будущем на нашей планете, возможно, вновь появится императорский дятел. В Государственном Дарвиновском музее уверены, что последние методы молекулярной биологии позволяют выделить и воспроизвести ДНК этих птиц.
-
-
Дронт

-
В июне 2006 года голландские учёные обнаружили на острове Маврикий хорошо сохранившиеся останки дронта — вымершей исторически недавно (в XVII веке) нелетающей птицы. Ранее наука не располагала останками птицы, в исчезновении которой, как всегда, виноват человек. Но теперь появилась определенная надежда на «воскресение» удивительного представителя пернатых.
3.4Клонирование гигантских птиц
Планы по клонированию исчезнувших гигантских птиц были поставлены под сомнение в результате исследований учёных Оксфордского университета. Выделив участки ДНК из останков вымерших птиц, ученые обнаружили, что их генетический материал настолько разрушен, что современная технология не позволяет провести полноценное клонирование. Цель научных работ состояла в возрождении вымерших несколько веков назад новозеландского страуса Моа, а также Мадагаскарского эпиорниса (птицы-слона).
Образцы ДНК были взяты из фрагментов тканей, сохранившихся в музеях. Однако ученые не смогли получить достаточную по своей длине цепочку ДНК, чтобы провести клонирование. Тем не менее, некоторые ученые считают, что в ближайшие годы будет разработана технология восстановления утраченных частей ДНК, путем вшивания туда «заплат» из ДНК близкородственных видов.
4.Применения клонов животных
Клоны не всегда выглядят одинаково. Хотя у клонов один и тот же генетический материал, окружающая среда так же играет огромную роль в том, как приспособится к ней организм клонированного существа. К примеру, первая кошка, которая была клонирована, ее звали Сиси, была каленкорской породы и была совсем не похожа на свою мать (донора) .
Репродуктивное клонирование может позволять исследователям клонировать животных с потенциальной выгодой для областей медицины и сельского хозяйства. Например, те же самые Шотландские исследователи, которые клонировали Долли, клонировали другую овцу, которая была генетически модифицирована, чтобы давать молоко, которое содержит человеческую основу белка для крови . В дальнейшем этот белок может отбираться из молока и подаваться человеку в чистом виде, это очень поможет людям, у которых низкая свертываемость крови. Так же можно использовать животных для того чтобы тестировать на них новые виды лекарств и обычную продукцию, предназначенную для человека. Большое преимущество использования клонированных животных для проверки на таблетки состоит в том, что все они являются генетически идентичными, что означает, что их реакция на таблетки должна быть боле менее сходной, чем у животных с различным генетическим набором.
Другой причиной для клонирования может служить то, что существуют популяции животных, которые стоят на грани вымирания. В 2001 году именно по этой причине ученые произвели первого клона, подвергнутого опасности вымирания — азиатского вола.
Детеныш, который развивался в матке у своей мамы-заместителя погиб всего лишь через три дня после своего рождения. Этот опыт был перенят и уже через два года, в 2003 году, ученые создают клон особи вола, так же стоящего на грани исчезновения. Вскоре 3 африканских диких кошки были клонированы из замороженных эмбрионов, которые были использованы в качестве ДНК.
Некоторые люди так же проявили интерес в том, чтобы их умерших домашних любимцев клонировали, надеясь, что эти клоны будут абсолютно такими же как и их умерший донор. Но как показало клонирование Кошки Сиси, клон не всегда выглядит так же, как и его «оригинал», у которого было взято ДНК .
Заключение
Клонирование – процесс создания генетически сходного организма неполовым путем. Клонирование использовали много лет для выращивания растений. Животное клонирование было предметом изучения для ученых многие годы, но получало мало внимания до 1997, пока не было клонировано первое млекопитающее — овечка Долли. Ученный Долли и несколько других ученых клонировали различных животных, включая коров и мышей. Недавний успех клонирования привел к жестким дебатам среди ученых, политиков и широкой публики об использование и этике клонирования животных и возможно человека.
За последние 50 лет, ученые провели эксперименты по клонированию в обширном круге животных, использовав много различных методов. В 1979, исследователи произвели первых генетически идентичных мышей, расколов эмбрион мыши в экспериментальной трубе, а затем внедрив получившийся эмбрион в матку взрослой самки мыши. Вскоре после того, как исследователи произвело первых генетически идентичных коров, овцу и цыплят, перемещая ядро клетки, взятой у раннего эмбриона в яйцо, у которого было освобождено ядро.
Главная причина клонирования животных в том, чтобы произвести организмы с определенными качествами, которые необходимы человеку, например овца была выведена чтобы предоставить человеческий инсулин. Если бы ученые полагались только на половое (сексуальное) размножение чтобы вывести этих животных, они бы рисковали тем, что необходимые им качества исчезли, так как половое размножение (сексуальное) переставляет генетический код в блоках. Другими причинами для клонирования могут быть потерянные или умершие домашние животные или животные, которые находятся на грани вымирания. Какими бы не были причины, новые технологии клонирования разожгли много этических спорах среди ученых. Некоторые государства рассмотрели или предписали законодательство, чтобы замедлить, ограничить или запретить эксперименты клонирования. Ясно, что клонирование будет частью нашей жизни в будущем, но будущее этой технологии должно всё же быть определено.
Список литературы
1. С.И.Заир – Бек, И.В.Муштавинский, Развитие критического мышления на уроке, — М.; Просвещение,2004.
2. Газета «Биология» Издательского дома «Первое сентября», № 12/2003.(Л.В. ЯКОВЕНКО Медицина и клонирование)
3. Газета «Биология» Издательского дома «Первое сентября», № 30/2003.(Голем третьего тысячелетия. Религиозные и исторические последствия клонирования)
4.Газета «Первое сентября» Издательского дома «Первое сентября», № 12/2003 ( Василий ЧЕШИРСКИЙ.Самая тонкая цепочка. Что такое клонирование с биологической точки зрения?)
5.Газета «Первое сентября» Издательского дома «Первое сентября», № 15/2003. (А.ВОЛКОВ. Клонирование: мертвый сезон)
6. Газета «Первое сентября» Издательского дома «Первое сентября», № 15/2003.(А.ГРУДИНКИН, Рождены по ошибке. Клонированные организмы чаще всего нежизнеспособны. Почему?) 7. Афонькин С. Ю. Долли бросает вызов, или размышления о клонировании людей. Биология. N 6, 1999.
8. Бутенко Р. Г. Биология клетки и биотехнология. Наука и человечество, 1987.
9. Дейвор Сольтер. Разведение овец путем пересадки клеточных ядер. Биология. N 38, 1997.
10. Кот М. М. Селекция животных. Перспективы развития. Биология в школе. N 2, 1991.
11. Преждевременное старение Долли (обзор журнала «Nature»). Знание-сила. N 9-10, с. 10, 1999.
12. Рувинова Э. И. Еще раз о клонировании. Биология. N7, 1998.
13. Чижиков Максим. Клонирование, сэр! Комсомольская правда. 5 апреля 2000.
14. Чикин Максим. Овечка Долли стареет не по дням, а по часам! Комсомольская правда. 1999.
15. Чойрыш А. И. Правовые и этические проблемы клонирования человека. Государство и право. N 11, 1998, с. 87-93.
16. В.А.Струнников «Клонирование животных: теория и практика», «Природа», №7, 1998 г.
17. Е.В.Мохов. «В ЧЕМ СЕКРЕТЫ ДОЛГОЛЕТИЯ. ПОЧЕМУ МЫ ЖИВЕМ ТАК МАЛО?..»
18. Соровский образовательный журнал, 1999 №4, клонирование животных, Л.И.Корочкин.
19. Журнал «Человек», 1998 №3, Долли – случайность или закономерность? Конюхов Б.В.
20. Журнал «Свет: природа и человек», 1999 №1.
21. Журнал «Студенческий меридиан», 2001 январь.
22. Журнал «Природа», 1998 №7, клонирование животных: теория и практика Струнников В.А.
23. Афонькин С. Ягнята Франкенштейна //Химия и жизнь. — 1999. — № 3.
24. Краснопольская И. Медицина, которой мы не знали // Российская газета. — 2002. — №40 (2908).
25. Кирпанев В.П. Этика клонирования: жизнь или смерть? — Ставрополь, 2004.
26. Дягтерев Н.Д. Клонирование: Правда и вымысел — 128 с. Наука и жизнь: За гранью очевидного
Сколько стоит клонирование кошки или собаки?
Только вдумайтесь — со дня рождения клонированной овечки Долли в 1996 году прошло более двадцати лет! Создание клонов животных уже давно превратилось из фантастики в реальность и в мире уже существует множество биотехнологических компаний, предоставляющих такую необычную услугу. Как правило, их клиентами являются любители домашних животных, которые хотят видеть своих любимцев даже после их смерти. Одной из таких компаний является китайская Sinogene Biotechnology, в лаборатории которой недавно родился клонированный котенок по кличке Чеснок. Биологи берут за работу довольно большие деньги, но это того стоит.

Компания уже проводила успешные клонирования собак, но кошками она занялась только в 2018 году. На недавней пресс-конференции в Пекине представители Sinogene Biotechnology объявили, что им наконец-то удалось создать клона кошки. Они не стали углубляться в подробности, а только сказали, что перенесли клетки требующей воспроизведения кошки в тело суррогатной матери. Спустя 66 дней после пересадки клеток, 21 июля 2019 года, мать родила точную копию домашнего животного. Котенку дали кличку Чеснок.
Кошка китайца по имени Хуан Ю
Первая клонированная кошка в Китае
Клонирование было сделано по заказу человека по имени Хуан Ю. По его словам, его домашняя кошка умерла от болезни мочевыводящих путей и ему очень хотелось, чтобы любимица всегда оставалась с ним, хотя бы в виде копии. Представители Sinogene Biotechnology уверяют, что клонированный котенок внешне точно похож на любимицу заказчика и отличия заключаются только в его характере. Впрочем, в будущем биологи хотят переносить воспоминания животных в клонированных особей при помощи искусственного интеллекта. Только вот как они это будут делать, опять же, они не спешат рассказывать.
Котенок Чеснок — клон, созданный в Китае
Сколько стоит клонирование?
Если компания действительно будет создавать точных клонов, у нее явно будет много клиентов. Если верить статистике, на данный момент в Китае насчитывается около 73 миллионов владельцев домашних животных. У некоторых из них живут разнообразные попугаи, пауки и даже змеи, но все же подавляющее большинство предпочитает кошек и собак. Идея «воскрешения» умерших животных при помощи клонирования кажется весьма заманчивой — давайте обсудим в нашем чате, воспользовались бы вы такой услугой?
В 2017 году Sinogene Biotechnology успешно клонировала собаку Лун Лун
Если да, то вам наверняка интересна цена клонирования. В статье про возможность создания копии самой грустной кошки в мире мы упоминали, что биотехнологические компании просят за услугу около 25 000 долларов. У компании Sinogene Biotechnology стоимость клонирования, по неизвестным причинам, гораздо выше и зависит от животного. Таким образом, за клонирование кошки компания просит 35 000 долларов, а за создание клона собаки — 54 000 долларов.
А что насчет клонирования людей? Мы готовы к этому?
Думаем, такая цена будет держаться недолго и будет постоянно расти. Мы уже упоминали, что в будущем компания хочет оснащать клонов воспоминаниями и характером погибшей особи при помощи искусственного интеллекта. А где вы видели, чтобы такие технологии стоили дешево? Возможно, полный «комплект» клонирования обойдется на несколько десятков тысяч долларов дороже. Впрочем, высокая стоимость клонирования не остановит истинных любителей домашних животных. Певица Барбара Стрейзанд, например, легко отдала за клонирование своего пса целых 50 000 долларов.
КЛОНИРОВАНИЕ ЖИВОТНЫХ
КЛОНИ́РОВАНИЕ ЖИВО́ТНЫХ, искусственное получение генетически идентичных организмов с помощью экспериментальных манипуляций с яйцеклетками (ооцитами) и ядрами соматических клеток животных in vitro и in vivo, подобно тому, как в природе появляются однояйцевые близнецы. Клонирование животных достигается в результате переноса ядра из дифференциированной клетки в неоплодотворенную яйцеклетку, у которой удалено собственное ядро (энуклеированная яйцеклетка), с последующей пересадкой реконструированной яйцеклетки в яйцевод приемной матери. Первые успешные опыты по клонированию животных были проведены в середине 1970-х гг. английским эмбриологом Дж. Гордоном (Gordon) в экспериментах на амфибиях, когда замена ядра яйцеклетки на ядро из соматической клетки взрослой лягушки привела к появлению головастика. Это показало, что техника трансплантации ядер из соматических клеток взрослых организмов в энуклеированные ооциты позволяет получать генетические копии организма, послужившего донором ядер дифференциированных клеток, и стало основанием для вывода об обратимости эмбриональной дифференцировки генома по крайней мере у земноводных. Однако долгое время все попытки применить описанный выше метод для клонирования млекопитающих были безуспешными. Значительный вклад в решение этой проблемы был сделан шотландской группой исследователей из Рослинского института и компании «PPL Therapeuticus» (Шотландия) под руководством Яна Вильмута (Wilmut). В 1996 появились их публикации по успешному рождению ягнят в результате трансплантации ядер, полученных из фибробластов плода овцы, в энуклеированные ооциты. В конечном виде проблема клонирования животных была решена группой Вильмута в 1997, когда родилась овца по имени Долли — первое животное, полученное из ядра взрослой соматической клетки: собственное ядро ооцита было заменено на ядро клетки из культуры эпителиальных клеток молочной железы взрослой лактирующей овцы.
В дальнейшем были проведены успешные эксперименты по клонированию различных млекопитающих с использованием ядер, взятых из взрослых соматических клеток животных (мышь, коза, свинья, корова). Появление технологии клонирования животных вызвало не только большой научный интерес, но и привлекло внимание крупных компаний и финансового бизнеса во многих странах. Подобные работы ведутся и в России, но целенаправленной программы исследований не существует.
В целом технология клонирования животных еще находится в стадия развития. У большого числа полученных таким образом организмов наблюдаются различные патологии, приводящие к внутриутробной гибели или гибели сразу после рождения.
Использование технологии клонирования предоставляет уникальную возможность получать фенотипически и генетически идентичных животных, которые могут быть использованы для решения различных теоретических и практических задач, стоящих перед биомедициной и сельским хозяйством. В частности, использование клонирования животных должно способствовать изучению проблемы тотипотентности диффренциированных клеток, развития и старения организмов, злокачественного перерождения клеток. Благодаря технологии клонирования появилась возможность ускоренной генетической селекции и тиражирования животных с рекордными производственными показателями. В сочетании с трансгенозом (см. Трансгенные животные (см. ТРАНСГЕННЫЕ ЖИВОТНЫЕ)) клонирование животных открывает дополнительные возможности для производства ценных биологически активных белков, используемых для лечения различных заболеваний человека. Клонирование животных позволит проводить испытания медицинских препаратов на идентичных животных. В медицине представляется перспективной клеточная терапия на базе использования клонированных клеток. Такие клетки должны компенсировать недостаток и дефект собственных клеток организма и, главное, не будут отторгаться при трансплантации. Технология клонирования животных позволит, по-видимому, осуществлять и широкомасштабную ксенотрансплантацию органов, т. е. замену отдельных органов человека на соответствующие органы клонированных животных.
В вопросе клонирования человека в настоящее время существует как техническая, так и большая этическая проблемы. В большом числе стран использование данной технологии применительно к человеку официально запрещено и преследуется по закону (США, Франция, Германия, Япония), причем во Франции, например, за эксперименты по клонированию человека предусмотрено тюремное заключение сроком до 20 лет. Это, однако, не исключает окончательно возможность ее использования в будущем, после детального изучения молекулярных механизмов взаимодействия цитоплазмы ооцита-реципиента и ядра соматической клетки-донора, а также совершенствования самой техники клонирования животных. В частности, в Англии уже разрешено проведение экспериментов по клонированию с использованием эмбриональных клеток человека. Вместе с тем надо помнить, что остается одно ясное и принципиальное ограничение, связанное с клонированием человека: интеллект человека клонировать нельзя.
Фото: Фотобанк Лори
12 января 1998 года 24 государства из 43 стран-членов Совета Европы подписал Дополнительный Протокол к Конвенции о защите прав человека и человеческого достоинства, запрещающий клонирование человека. 1 марта 2001 года после ратификации 5 странами этот Протокол вступил в силу. На данный момент – это единственный международный акт, регулирующий проблему. Так почему нельзя клонировать людей?
Разберемся в нюансах
В еврейской мифологии – Голем, в западноевропейской литературе — Франкенштейн. Человечество всегда занимала проблема создания живых существ в лабораторных условиях. Существование близнецов наталкивало на идею о возможности каким-либо способом получить точную копию реально существующих людей.
Зародившаяся в начале XX века новая научная дисциплина генетика продвинула человечество к пониманию процессов передачи у живых организмов наследственных признаков и формирования новых. Стартовавшие в 70-х годах прошлого века работы по расшифровке генома человека к началу нового тысячелетия позволили получить довольно точное представление о его структуре. В 90-е в научном сообществе сформировалось убеждение о принципиальной возможности клонирования человека.
Клон – условно точная копия некоего объекта. Термины «клон», «клонирование» первоначально использовались в микробиологии и селекции, после – в генетике, в связи с успехами которой и вошли в общее употребление.
Клонирование человека – это технология создания человеческого эмбриона и выращивание из него людей, чей генотип будет идентичен генотипу существующих сейчас или уже умерших индивидуумов. Необходимо только осознавать, что клон не может быть точной копией человека. При клонировании копируется только генотип, но не фенотип. Фенотип — совокупность внешних и внутренних признаков организма, приобретаемых в результате индивидуального развития. Сознание – в том числе.
История овечки Долли

Овечка Долли родила трех ягнят. 1999 год. Фото: ИТАР/ТАСС
В 1996 году произошло событие, которое и заставило заговорить о возможном клонирования людей. В Рослинском институте в окрестностях Эдинбурга Ян Вилмут и Кит Кэмпбэлл в ходе эксперимента смогли клонировать первое млекопитающее – овцу. Генетическая информация для процесса клонирования была взята из взрослых дифференцированных клеток умершего к тому времени животного. Овечку назвали Долли.
Пресса объявила о ее рождении только через семь месяцев – 22 февраля 1997 года. В дальнейшем в институте было клонировано еще четыре овцы, что подтвердило эффективность технологии переноса ядра клетки с генетической информацией в половую клетку-донор, из которой и развивается эмбрион. Долли прожила шесть с половиной лет, родила шестерых ягнят и умерла от прогрессирующего заболевания легких.
Эксперимент, который многие сравнивали с расщеплением атома, впоследствии подвергся серьезной критике. В научных изданиях появились материалы о том, что генетическая информация донора в действительности не была полностью удалена из полученной яйцеклетки и Долли оказалась носителем генов двух животных. А это уже совсем не клон.
Проблемы клонирования

Фото: ИТАР/ТАСС
Итак, теоретически можно попробовать клонировать человека. Но возникает вопрос – зачем? Тем более, что, как мы уже отмечали, точной кальки не получится. А к возможности копировать сознание современная наука даже близко не подошла. Поэтому воспроизвести Пушкина, Толстого, Эйнштейна или Мерилин Монро при всем желании не выйдет.
В головах отдельных фантастов и футурологов от медицины на это счет возникла идея о клонах – источниках донорских органов. Но эта идея тут же наткнулась на шквал критики. Она оказалась неприемлемой для общества с позиций религиозных, этических, социально-нравственных, юридических. Как результат – во многих странах мира возможное репродуктивное клонирование человека попало под запрет. Более того – идет криминализация процесса. В уголовные кодексы этих стран включены статьи, карающие за попытку создать человеческую копию.
Но есть еще и «терапевтическое клонирование». Его суть состоит в том, что возможно прервать развитие полученного в результате клонирования эмбриона в первые 14 дней и использовать его для получения стволовых клеток. Подобная процедура разрешена в США, Великобритании и некоторых других странах. Тем более, что методики, используемые при терапевтическом клонировании, широко применяются при исследованиях заболеваний, передающихся на генетическом уровне. Так, по мнению Шухрата Миталипова — известного биолога, работающего сейчас в США над проблемами генетических заболеваний – запрет на манипуляции с эмбрионами, ядрами половых и соматических клеток серьезно осложняет такую работу. Лаборатории Миталипова первой в мире удалось создать технологию редактирования генома человеческого эмбриона с кардиомиопатией. Ученый рассчитывает на то, что лет через 10-15 понимание необходимости подобных исследований приведет к серьезным положительным подвижкам и избавит ученых, работающих с человеческими эмбрионами, от надуманной критики.
А что в России?

Фото: Садиков Рамиль/ РИА Новости
РФ формально не присоединилась к Протоколу к Конвенции о защите прав человека и человеческого достоинства. Но клонирование человека временно запрещено Федеральным законом № 54-ФЗ от 20 мая 2002 г. «О временном запрете на клонирование человека».
Первоначально срок действия запрета ограничивался пятью годами. Но затем в текст закона были внесены поправки, продлевающие его на неопределенное время. При этом закон запрещает репродуктивное клонирование и не касается клонирования терапевтического.
Сегодня в России нет научных центров, способных на уровне, сопоставимом с мировым, работать над проблемами трансплантации клеточных ядер. И здесь мы серьезно отстаем не только от США и Великобритании – мировых лидеров. В последние годы большие ресурсы на исследования в этом направлении стал выделять Китай.
И всё-таки
Знаменитый британский биолог, лауреат Нобелевской премии Джон Гордон, чьи работы по клонированию шпорцевой лягушки в конце 50-х – начале 60-х годов XX века легли в основу современных методов трансплантации клеточных ядер, считает, что в ближайшие 50 лет человечество все же станет свидетелем клонирования человека. «Даже к методике искусственного оплодотворения относились с крайней подозрительностью, когда она была только создана. Но после рождения в 1978 году Луизы Браун, первого «ребенка в пробирке», общество смогло принять технологию», — считает ученый. Время покажет, окажется ли он прав. Пока информации о успешных попытках клонирования ни у научного сообщества, ни у прессы нет.
Сергей Анисимов
